Em nossas postagens anteriores, estudamos sobre os diferentes tipos de ligações químicas (acesse a postagem clicando aqui!). Nesta postagem, você pôde estudar basicamente sobre as ligações iônicas, covalentes e também sobre as ligações metálicas. Entretanto, as ligações covalentes podem ocorrer de diferentes formas. Assim sendo, o objetivo de nossa postagem de hoje é explicar os diferentes tipos de ligações covalentes.
Antes de mais nada, vamos relembrar o que são as ligações covalentes. As ligações covalentes são aquelas em que os átomos compartilham elétrons entre si, ou seja, ao invés de transferirem os elétrons de um para outro, compartilham o mesmo elétron, tornando-se assim estáveis.
De maneira geral, as ligações covalentes costumam ocorrer em elementos que apresentam entre 4 e 7 elétrons em sua camada de valência. Normalmente, essa ligação ocorre entre elementos não metálicos. Todavia, existe a possibilidade da ocorrência destas ligações entre metais e metais, ou ainda metais e ametais. No entanto, como falamos, essas ligações ocorrem com uma frequência muito menor.
Os tipos de ligações covalentes que vamos estudar são: ligações simples, duplas, triplas e covalentes dativas. Vamos observar cada uma delas nos tópicos abaixo.
Indice
Ligações covalentes simples
Nas ligações covalentes simples, ocorre o compartilhamento de apenas um elétron por cada átomo. Desta forma, amos os elementos estarão estáveis segundo a “regra do octeto”. Essas ligações são comuns entre elementos que apresentam 7 elétrons em sua camada de valência. Veja a seguir a representação dos elétrons na ligação realizada entre uma molécula de hidrogênio e uma molécula de cloro, com o objetivo de formar o ácido clorídrico:

Como havíamos mencionado acima, observe a presença de 7 elétrons na camada de valência do cloro, sendo que sua estabilização é dada com 8 elétrons, enquanto o hidrogênio possui um elétron em sua camada de valência e é estabilizado com dois elétrons.
Ligação covalente dupla
O funcionamento das ligações covalentes duplas ocorre da mesma maneira das ligações simples, ou seja, através do compartilhamento de elétrons. No entanto, nas ligações duplas cada elemento pode compartilhar dois elétrons para garantir a sua estabilização. Um exemplo deste tipo de ligação ocorre da união entre duas moléculas de oxigênio, para a formação de O2. Veja a seguir uma representação deste tipo de ligação:

Como havíamos adiantado, nestas ligações ocorre o compartilhamento de dois elétrons por cada elemento.
Ligação covalente tripla
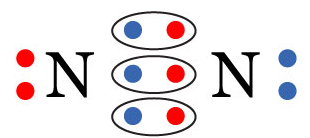
Agora você já deve ter desvendado o que acontecerá na ligação tripla! Nestas ligações, cada elemento compartilha 3 elétrons com o objetivo de se tornarem estáveis. Um exemplo típico destas ligações ocorre na formação de nitrogênio (N2), que são ligados da seguinte maneira:
Ligações covalentes dativas
As ligações covalentes dativas, ou coordenadas, são aquelas onde os átomos dividem os elétrons dividem elétrons em sua camada de valência, e os átomos que sobram são “doados” para outra molécula. Um exemplo comum destas ligações está na formação de dióxido de enxofre (SO2), onde ocorre uma ligação dupla (1°) seguido do compartilhamento dos elétrons do enxofre (2°).

Desta maneira, estudamos os quatro diferentes tipos de ligações covalentes. Entender como cada uma destas reações ocorrem é muito importante para a resolução de questões que envolvem reações, fundamentais para a química no Enem!



1 comment