O estudo da termodinâmica é importante em diversas áreas. Seus conceitos são utilizados, por exemplo, para projetar equipamentos que fazem processamentos térmicos de metais ou alimentos nas indústrias. Mas ela pode estar mais próxima do nosso cotidiano do que imaginamos, sendo a panela de pressão é outro exemplo da aplicação de seus conceitos que com certeza já usamos ou pelo menos temos em casa.
A termodinâmica envolve o estudo do calor, trabalho e outras formas de energia e é essencial para garantir uns pontinhos a mais no ENEM.
A primeira lei da termodinâmica nada mais é que uma lei de conservação de energia. Ela relaciona a quantidade de calor fornecida ao sistema com a variação de energia interna e a geração de trabalho.
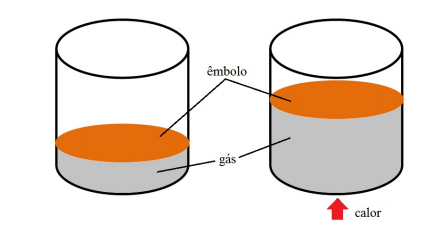
Já sabemos que, ao aquecermos um gás, ocorre a agitação das moléculas que o compõem, ou seja, a elevação da temperatura gera um aumento da energia interna do gás. Supondo que o mesmo esteja contido em um recipiente que possui um êmbolo que pode se mover, quando colocamos uma fonte de calor próxima ao recipiente estamos aquecendo o gás, fazendo sua energia cinética aumentar e levando a um aumento de pressão que empurrará o êmbolo para cima, como é possível observar na figura 1.
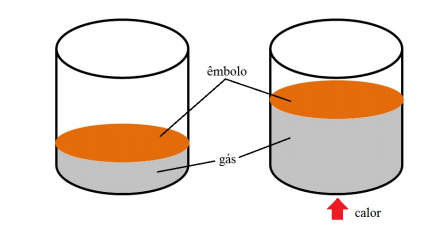
O deslocamento do êmbolo ocorre devido a um trabalho (Ʈ) realizado pelo gás. O aumento da energia cinética gera um aumento da pressão dentro do recipiente e uma força empurra o êmbolo para cima.
A partir dessas informações, chegamos á expressão conhecida como a primeira lei da termodinâmica, descrita a seguir:
Q = Ʈ + ΔU
Onde Q é o calor fornecido ao sistema, o Ʈ é o trabalho realizado pelo gás e ΔU é a variação da energia interna ocasionada pelo aquecimento.
Numa situação em que, ao invés do gás receber calor ele cede o calor, o contrário ocorre, ou seja, a sua temperatura cai, sua energia interna diminui e o trabalho é negativo, pois o êmbolo abaixa ao invés de subir, como no caso visto anteriormente.